このページでは、このように色づけされた用語をクリックすると➤用語解説窓が開きます。
また、頭に★マークのついた単語(あるいは文)をクリックすると、関連する外部リンクへ移動します。
2020年初頭に新型コロナウイルスが猛威を振るいだした時、人体にも手軽に使えることで良く知られていたアルコール消毒液が店頭から消え失せ、 医療関係施設でも入手困難になって大変な騒ぎになりました。
そんな時、次亜塩素酸水がアルコール消毒液の代わりに使えるという話が広まりましたが、 「これはすばらしい」という肯定的意見があれば「いや、本当に効果があるのか疑問だ」という否定的見解もありました。 一時は国の研究機関や大学から、製造企業や一般市民まで巻き込んだ論争になった程です。
最終的に、2020年6月26日に(独)製品評価技術基盤機構が★ 正しく使用すれば有効であるという報告を出したので、 現在のところ論争自体は落ち着いたように見えます。
とはいうものの、インターネットで検索すると「次亜塩素酸xx」という類の商品が数多くあり、 それぞれについての説明も微妙に異なっています。 実際のところ、詳細に調べれば、同じ「次亜塩素酸水」という言葉で説明されている商品でも、 その成分や効能、安全性や使い勝手などがずいぶん異なったり、科学的に見て首をかしげたくなるような商品説明が見受けられたりしました。 このような事態を受けて、2020年から2021年にかけて、景品表示法に基づく措置命令が消費者庁から複数の次亜塩素酸水販売事業者に出されました。 そして、2022年3月には化学的調製により製造される「次亜塩素酸分子水溶液」のJSA 規格が発行されましたので、 次亜塩素酸水の効力を過剰に謳うような商品説明はかなり少なくなったように見えます。
しかし今(2022年9月現在)でも、世界的大手のwebマーケットで、直接人体に用いる場合の安全性が確認されているとは言えない500ppmという高濃度の次亜塩素酸水商品が充分な取扱説明なしで販売されているのを見かけます。 (株)アクトも次亜塩素酸水である「クリーン・リフレ」を商っていますので、 お客様には次亜塩素酸水の特徴、安全性、効果、取扱い上の注意等々について説明する義務があると考えています。 ですからこれ以降は、科学的な観点に立って、大学や研究機関などの試験研究結果を調べた上で、 アクト自身の知見も付け加えて、次亜塩素酸水の効果や取扱上の注意事項、そして製造方法などについて解説していきたいと思います。
次亜塩素酸水とは一体どういうものなのでしょう? 聞いたことはあるけど、よくわからないという方が多いのではないかと思いますので、まずその辺からご紹介していきましょう
次亜塩素酸水の定義
一般名詞としての次亜塩素酸水に定義はありません。つまり、組成範囲などが明確に定められているわけではありません。社会通念的に解釈すれば、食塩が溶けている水を食塩水というのと同じように、次亜塩素酸(分子式 HClO)が溶けている水を次亜塩素酸水といいます。科学的に表現すれば、食塩水は「塩化ナトリウム水溶液」で次亜塩素酸水は「次亜塩素酸水溶液※」となります。
一方、法規的には、「厚生労働省により指定された食品添加物(殺菌料)としての次亜塩素酸水」と「農林水産省により指定された特定農薬としての次亜塩素酸水」の製造方法および化学組成範囲などの規定が国によって定められていますので、化学的調製により製造される次亜塩素酸水を食品添加物や特定農薬として用いることはできません。
食品添加物(殺菌料)としての次亜塩素酸水については、平成21年8月19日に開催された厚生労働省の
薬事・食品衛生審議会食品衛生分科会乳肉水産食品部会配付資料として:
資料4-1 生食用鮮魚介類の加工への次亜塩素酸水の使用に関する要望書
資料4-2 次亜塩素酸水と次亜塩素酸ナトリウムの同類性に関する資料
資料4-3 新しい殺菌・酸性電解水
資料4-4 次亜塩素酸水の食品添加物指定に関連する資料
★ 食品安全委員会評価書 次亜塩素酸水
といった資料が公開されています。
これらのうち「食品安全委員会評価書 次亜塩素酸水」には食品添加物(殺菌料)としての次亜塩素酸の規定が詳述されています。また「次亜塩素酸水の食品添加物指定に関連する資料」には「次亜塩素酸水そのものは流通しない」と記載されています。 つまり所定の原料を所定の方法で電気分解により製造し、製造直後に用いる場合のみ食品添加物としての次亜塩素酸水とみなされます。
特定農薬としての次亜塩素酸水については農林水産省が各都道府県知事宛に出した★通達の別紙1~別紙4をご覧ください。基本的な製造法などは厚生労働省の規定を踏襲していますが、大きな違いは電気分解する原料が「塩酸又は塩化カリウム水溶液」であって、塩化ナトリウムを用いてはいけないことです。これは農地に塩害を生じさせないための配慮と想定されます。
次亜塩素酸の歴史
アメリカ合衆国のBurk Hart社のwebサイトには次のように書かれています(★原文はこちらにあります):
1811 年、鉱夫安全ランプで有名な Humphry Davy 卿によって、次亜塩素酸は感染と闘うために身体が生成するものだと明らかにされました。
1823年、Humphry 卿の学生であるMichael Farradayは、生理食塩水に電流を流して電気分解することによってHOCLを分離することに成功しました。
HOCLはこの後で紹介するHClOつまり次亜塩素酸のことです。しかい、この記述には一部間違いがあるようで、「★実験の天才ファラデーの日誌(木原、2013)」によると、ファラデーは1813年以降 Davy 卿の助手をつとめ、1823年に塩素の液化に成功し、1825年には王立研究所実験室の主任に昇格しています。そして、1832年末以降に本格的に電気分解の実験を開始しています。
さらに「★ファラデーの電気分解実験、1833」という有名な絵が残っています。ですからBurk Hart社のサイトの記述は「1833年Humphry 卿の助手である」と修正する必要がありそうです。
どちらにしても、あのマイケル・ファラデーが190年も前に食塩水を電気分解して次亜塩素酸を造っていたとは!…
でもそういえば★ファラデーの法則とは「ファラデーの電磁誘導の法則」と「ファラデーの電気分解の法則」の2本立てだったはずです。
ファラデーが電気分解の実験を行う際に何種類かの電解質を用いたと思いますが、最も身近な電解質である塩化ナトリウム(食塩)を用いなかったはずはありません。
ではファラデーが造った次亜塩素酸とはどのようなものだったのでしょうか。土壌粒子によるイオン交換作用を発見したのが1845年のことですから、イオン交換膜が手に入る時代ではありませんので、上記「ファラデーの電気分解実験」に描かれているような最も基本的な1室型の電気分解装置で造ったものだったのでしょう。であれば、弱アルカリ電解生成水 (いわゆる電解次亜水)に違いありません。Burk Hart社のサイトには、この他にも「HOCL は第一次世界大戦中の傷の洗浄に使用され、 これで治療を受けた兵士は受けていない兵士の半分の時間で回復した」ことや、「HOCL は急速に劣化するので使用時に生成する必要があり、そのためにフィールド ラボを設置する必要があった」など、興味深いことが書かれています。 「フィールド ラボ」ということは戦場で次亜塩素酸水溶液(おそらく電解次亜水)を製造していたということでしょう。
次亜塩素酸の化学的基礎知識
理科の授業などで塩酸やクエン酸(の入った容器)を見たことがあると思いますが、次亜塩素酸を学校で見たという記憶はないと思います。 その理由にひとつは次亜塩素酸の不安定さにあります。 同じ理由により、第一次大戦中に次亜塩素酸を製造するために「フィールド ラボ」を設けなければならなかったのでしょうし、 つい最近まで広く一般に使用されることがなく、みなさんの目にとまることもなかったのでしょう。
ほぼ全てのみなさんが理科の授業などで一度は目にしたことがある塩酸は塩化水素(HCl)を水に溶かしたものです。 その塩化水素の水素(H)と塩素(Cl)の間に酸素(O)が割って入ったものを作ると次亜塩素酸の分子になります(下図)。
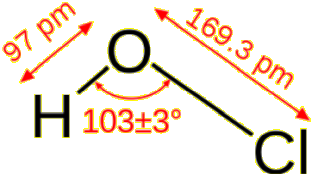
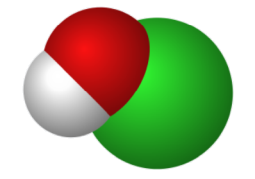
次亜塩素酸の分子構造とそのイメージ(白は水素の、赤は酸素の、緑は塩素の原子)
pm(ピコメートル)は1×10-12メートル。
★出典:ウィキペディア 次亜塩素酸
上の図の塩素原子を水素原子で置き換えると水(H2O)の分子と同じ並びになることにお気づきでしょうか。水の分子は電子を引き寄せやすい酸素原子1個に電子を奪われやすい水素原子2個が結合したものです。塩素は本来電子を引き寄せやすい原子であるのに、次亜塩素酸分子の中では水素原子の代役を果たしているように見えます。塩素原子が本来の性質に合わない役目を果たしているため、この後説明するように、次亜塩素酸分子はとても不安定で壊れやすいため水中でしか長時間は存在できません。しかし、その壊れやすさが次亜塩素酸の強力な破壊力の源になっているのです。
実は、私たちの体の中で好中球(白血球の一種)が次亜塩素酸を作り出し、菌・細菌やウイルスなどの病原体を攻撃するのに用いています。例えば ★奈良女子大の藤井先生の報告(2018)をご覧ください。
イメージ的にはこんな感じです ↓
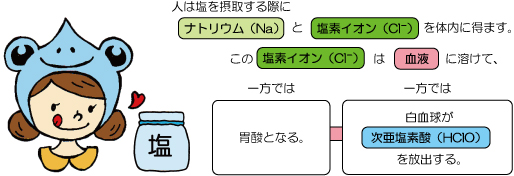
また、水道法では「遊離残留塩素を0.1mg/L※(結合残留塩素の場合は0.4mg/L)以上保持するように塩素消毒をすること」と決められていますが、この遊離残留塩素というのが実は次亜塩素酸(HClO)とそれが水中でイオンに解離した次亜塩素酸イオン(ClO-)を合わせたものなのです。

次亜塩素酸 HClO の効力は相手を酸化させることで発揮されます。 次亜塩素酸が酸素を受け取りやすい(酸化されやすい)有機物などに触れると:
HClO → HCl + O
というように分解して、相手に酸素を無理やり与える(酸化させる)反応がおきます。 結果として次亜塩素酸が消滅すると同時に、相手の有機物の一部が酸化により破壊されます。
各種病原体、生体の一部、アルコールなどの有機分子類は比較的酸化されやすい有機物なので、次亜塩素酸と反応します。 一方、常温では酸化されにくいプラスチックなどは次亜塩素酸水と接触しても簡単には酸化・分解されません。 したがって次亜塩素酸水をペットボトルに入れておいても、たちどころに効力を失うことは起こりません。
次亜塩素酸は微生物を破壊
次亜塩素酸分子は電気的に中性な(電荷を帯びていない)ため、菌・細菌などの細胞膜を通過して細胞の内側から微生物の中枢である細胞核などを破壊できます(下図)。城壁を魔法のように素通りして敵を攻撃するわけですから、敵もたまったものではありません。
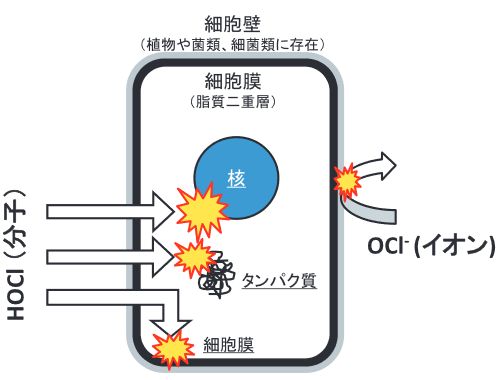
電荷を帯びていない次亜塩素酸分子は細胞膜を通過できる
(この図では次亜塩素酸をHOCl、次亜塩素酸イオンをOCl-と表記しています)
★出典:細菌・ウイルス等微生物に対する次亜塩素酸水の効果とその活用(中村ほか、2017)
一方、例えば次亜塩素酸ナトリウム(NaClO)が水に溶けた時の有効成分である次亜塩素酸イオン(ClO– あるいは上図のように OCl– と表わすこともあります)は負の電荷を帯びているため、細胞膜を通過できません。 ですから、細胞膜を破壊して微生物を殺すことになりますが、そのためには高濃度のClO-イオンが必要となります。
一般には次亜塩素酸(HClO)の殺菌・除菌力は次亜塩素酸イオン(ClO–)の約80倍と言われています(★「次亜塩素酸水と次亜塩素酸ナトリウムの同類性に関する資料」、厚生労働省、2009)。細胞の内側に入りこんで要所を責める次亜塩素酸の方がはるかに強い破壊力を持つということです。
下表は有効塩素濃度40mg/Lの次亜塩素酸水が有効塩素濃度1,000mg/Lの次亜塩素酸ナトリウム溶液よりも強い殺菌活性を持っていることを示しています。
| 微生物・ウイルス | 次亜塩素酸水 (40mg/L) | 次亜塩素酸Na (1,000mg/L) | |
|---|---|---|---|
| グラム 陽性菌 | 黄色ブドウ球菌 (Staphylococcus aureus) | ◎(10秒) | ◎(10秒) |
| MRSA (メチシリン耐性ブドウ球菌) | ◎(10秒) | ◎(10秒) | |
| セレウス菌 (Bacillus cereus) | △(3〜5分) | △(3〜5分) | |
| 結核菌 (Mycobacterium tuberculosis) | △(2.5分) | ▲(30分) | |
| その他の抗酸菌 | △(1〜2.5分) | ▲(2.5〜30分) | |
| グラム 陰性菌 | サルモネラ菌 (Salmonella Enteritidis) | ◎(10秒) | ◎(10秒) |
| 腸炎ビブリオ菌 (Vibrio parahaemolyticus) | ◎(10秒) | ◎(10秒) | |
| 腸管出血性大腸菌 (Escherichia coli O157:H7) | ◎(10秒) | ◎(10秒) | |
| カンピロバクター菌 (Campylobacter jejuni) | ◎(10秒) | ◎(10秒) | |
| 緑膿菌 (Pseudomonas aeruginosa) | ◎(10秒) | ◎(10秒) | |
| ウイルス | ノロウイルス (ネコカリシウイルス) | ◎ | ○ |
| インフルエンザウイルス (2009年新型含む) | ◎(10秒) | ◎(10秒) | |
| エンテロウイルス | ◎(10秒) | ◎(10秒) | |
| ヘルペスウイルス | ◎(10秒) | ◎(10秒) | |
| 真菌 | カンジダ (Candida albicans) | ◎(10秒) | ◎(10秒) |
| 黒カビ (アスペルギルス; Aspergillus niger) | △(5分) | ×(120分) | |
| 青カビ (ペニシリウム; Penicillium cyclopium) | △(5分) | ×(120分) | |
| 殺菌・除菌効果または不活化効果: ◎(即効)>○>△>▲>×(無効) | |||
表1: 酸性電解水(次亜塩素酸水)の殺菌活性
★出典:機能水研究振興財団
ウイルスを攻撃する次亜塩素酸のイメージ
強力な破壊力があるとはいえ、一個の次亜塩素酸分子が放出するのは一個の酸素原子だけですから、それで破壊できるのは病原体のごく一部分です。
自分自身よりはるかに大きなウイルスや細菌を不活化させるにはそれなりの量の次亜塩素酸が必要なので、有効塩素濃度※1が低い(次亜塩素酸の含有量が少ない)場合は効果が少ないということになります。実際に、NITEの報告によると、CoVID-19に対して十分な効力があったのは有効塩素濃度が35mg/L以上の次亜塩素酸水でした※2。
※1 殺菌や漂白などの強い反応を引き起こすことのできる塩素化合物中の塩素を「有効塩素」といいます。次亜塩素酸水の場合は次亜塩素酸分子、次亜塩素酸イオン、塩素分子の3種類の化合物について反応相手を酸化する能力を合計し、それと同じ酸化力をもつ塩素分子の濃度に換算したものが有効塩素濃度となります。次亜塩素酸水中には他にも塩化水素や塩化ナトリウムなどの塩素を含む成分が存在しますが、これらの成分中の塩素は有効塩素とは見なされません。従って次亜塩素酸水の「有効塩素濃度」と「塩素濃度」は異なったものとなります。
※2 通常の手指の消毒などを想定して行った試験の結果、35mg/L以上あればアルコール消毒液と同程度の効果が期待できると判断したものです。35mg/L以下では全く効き目がないということではなく、逆に35mg/L以上であればどのような用い方をしても確実に効果があるということでもありません。薄めの濃度のものでも量を多くもちいることにより濃いものと同等の除菌効果を得ることが可能です。
では、確実に効力のある有効塩素濃度50mg/Lの次亜塩素酸水がCoVID-19の感染の主因子となっている唾液中のウイルスと戦う場面をイメージしてみましょう。
CoVID-19を他人に感染させる可能性のある患者の唾液1mL中には100万個ほどのウイルスが含まれていると考えられています。 容積1mLの中に100万個のウイルスが均一に分布しているとすると、その平均間隔は 0.1mm(100,000nm)です。 この距離はコロナウイルスの大きさ(約100nm)の1,000倍にもなり、もしこれが身長1.7mの人間であれば、すぐ隣の人が1.7kmも離れていることになります。 感染を防ぐためには「三密」を防ごうと言われていますが、ウイルス自体は意外と「密」ではないようです。
一方、計算してみると、有効塩素濃度50mg/Lの次亜塩素酸水1mL中には4.25 x 1017 個の次亜塩素酸分子があることになり、分子が均等に分布しているなら、その間隔は13.3nmとなります。 さらに計算すると、新型コロナウイルスと同じ体積の中に400個ほどの分子があることになります。 もし、ウイルスを攻撃できる次亜塩素酸分子は直径100nmのウイルスの表面から10nm以内にある次亜塩素酸分子と仮定すれば、その範囲内にある分子の数はおよそ300個となります。 例えばそのうち100個が内部に潜り込んで様々な個所を破壊すれば、ウイルスを不活化するには十分だと考えて良いでしょう。 もし有効塩素濃度が0.5mg/L(水道水程度)であればウイルスの表面から10nm以内には3個の次亜塩素酸分子しかなく、500倍の大きさのウイルスに立ち向かうにはちょっと厳しい気がします。
500倍という大きさの違いは、人間とブヨの比率とほぼ同じです。 ブヨにまとわりつかれた場合を想像してみてください。 同時に三匹のブヨに襲われた場合は厄介ですが、それで殺されるようなことにはなりません。 しかし、実際には決して起こらないことですが、何百匹ものブヨがあなたの体内に入って内臓を攻撃した場合、結果は恐ろしいことになるでしょう。 次亜塩素酸と病原体の組み合わせの場合、そのようなことが現実に起きるのです。

次亜塩素酸水の安全性については数多くの報告がありますが、最も信頼のおけるもののひとつである、食品安全委員会の添加物評価書(2007年1月、★こちらからダウンロードできます)の中の一節を以下に引用します:
次亜塩素酸水の安全性については、強酸性(pH2.5、有効塩素濃度50~60 mg/kg)及び微酸性(pH5.5、有効塩素濃度70mg/kg)次亜塩素酸水について多くの報告があり、その中で急性経口毒性試験、皮膚刺激性試験、急性眼刺激性試験、皮膚感作性試験、口腔粘膜刺激性試験、復帰突然変異試験及び染色体異常試験において、変化は認められなかったとされている。また、細胞毒性では、高濃度においてやや細胞の増殖が抑制されたが、他の市販の消毒薬と比較して毒性の少ないことを認めている。
ただし、この評価書は厚生労働省が指定する食品添加物としての規格を満たす次亜塩素酸水(下図)について書かれたものであることに注意してください。「次亜塩素酸水」と称して売られている商品であってもこの規格から外れているものについては安全性が不明と判断してよく、別途評価が必要になると思います。
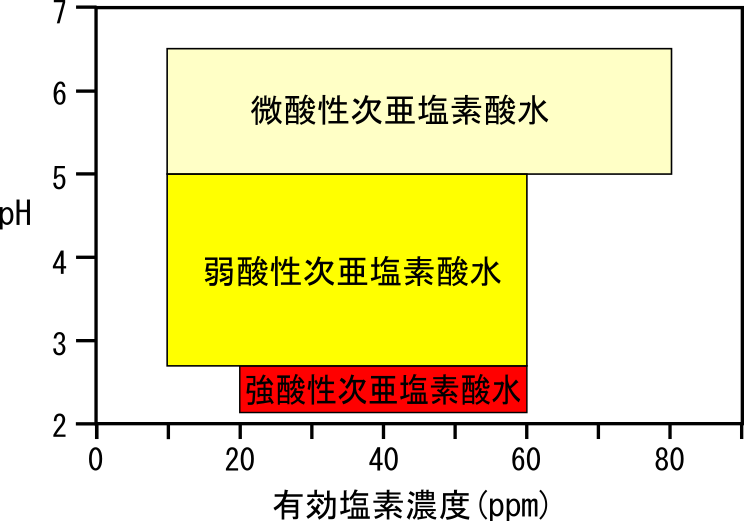
食品添加物としての次亜塩素酸水の組成範囲
厚生労働省の規定では、食品添加物としての次亜塩素酸水は、上の図に示された有効塩素濃度範囲とpH範囲を満たす必要があります。また、強酸性および弱酸性次亜塩素酸水は塩化ナトリウム水溶液の電気分解によって、微酸性次亜塩素酸水は塩化水素の水溶液(塩酸)もしくはこれに塩化ナトリウムを加えたものの電気分解によって製造されたものとされています。ここでは省略しますが、これら水溶液の濃度範囲についても決められています。厚生労働省が指定した以外の方法で製造された次亜塩素酸水を食品添加物として用いることはできません。
次亜塩素酸水の空中噴霧
新型コロナウイルスの感染拡大により次亜塩素酸水の空中噴霧についても話題になり、多くの議論がなされました。 「真水を噴霧して乾燥した室内空気中の湿度を50~60%程度まで高める」ことが新型コロナやインフルエンザ対策として有効であることに異論をはさむ人はいないと思います。次亜塩素酸水は水で薄めることにより有効塩素濃度をいくらでも下げることが可能です。もしたとえば、有効塩素濃度60mg/Lの次亜塩素酸水を空中に噴霧することが有害であるなら、有効塩素濃度がどこまで下がれば無害になるのでしょうか。また、人体に無害となる濃度ではウイルスに対する効果が全くなくなってしまうのでしょうか。もしそうであれば次亜塩素酸水の空中噴霧は意味がないことになりますが・・・・
実はその辺のことがまだ十分にはわかっていないのです。わからないうちは使用しない方が安全ということは理解できますが、危険なウイルスが身の回りにあるのであれば、使用した方が安全と考える人もいます。安全性テストが不十分なまま接種が開始された新型コロナワクチンについても同じようなことが議論されていますが、このような問題に関して私たちがいまやるべきことは、早く信頼のおけるデータを集めて、効果と危険性の両方を正確に判断できるようにすることだと思います。人体に無害で除菌できるという次亜塩素酸水の濃度範囲と噴霧量・噴霧方法などが明らかになれば、それだけで数多くの感染を避けることが可能となるでしょう。
世界保健機構が消毒薬を空中噴霧するのは危険であると警告したのは、実際に空中噴霧による被害が報告されたからでしょう。しかし、それは何か別の消毒薬一般についての話であって、WHOが次亜塩素酸水の噴霧の危険性を確認しているわけではありません。そしてまた、少なくとも日本国内では、次亜塩素酸水は消毒薬として扱われていません。
★2021年10月の厚生労働省から都道府県などへの事務連絡の別添には次のように書かれています。
問 厚生労働省・経済産業省・消費者庁特設ページ「新型コロナウイルスの消毒・除菌方法について」の「5.(補論)空間噴霧について」の【参考情報3】 において、「消毒効果を有する濃度の次亜塩素酸水を吸い込むことは、推奨できません。」としているが、これは厚生労働省として、次亜塩素酸水を空間に噴霧する事をいかなる場合でも禁止するという趣旨か
(答)
世界保健機関(WHO)は、新型コロナウイルスに対する消毒に関する見解の中で、 「室内空間で日常的に物品等の表面に対する消毒剤の(空間)噴霧や燻蒸をすることは推奨されない」としており、 このような国際的な知見に基づき、健康影響のおそれのある消毒剤や、 その他ウイルスの量を減少させる物質について、人の眼や皮膚に付着したり、 吸い込むおそれのある場所での空間噴霧をおすすめしない、という趣旨を示すものです。
なお、個々の製品の使用に当たり、その安全性情報や使用上の注意事項等を守って適切に使用することを妨げるものではありません。 ただし、「消毒剤や、その他ウイルスの量を減少させる物質」に該当する製品が、健康影響のおそれがあるものかどうかについては、 各製品の安全性情報や使用上の注意事項等を確認いただき、消費者に御判断いただくものと考えております。
要するに、人のいる空間への次亜塩素酸水の噴霧は健康影響のおそれが無いと言い切れないので、自己責任で使ってくださいということなのでしょう。 実際のところ、次亜塩素酸水(次亜塩素酸ナトリウム水ではありません)の空中噴霧に関して、危険であることを示すデータは見かけたことがありません。安全性と有効性を裏付ける資料については、例えば★(社)次亜塩素酸水溶液普及促進会議がとりまとめています。
ACT SNFの「外部資料リスト」では、次亜塩素酸水の空中噴霧実験について次のような文献と記事を列記してありますので、興味のある方はぜひご一読ください:
- (原文は英語)物体表面上のヒトノロウイルスの不活化に、液状および霧状の次亜塩素酸水溶液Steriloxを用いるための評価
- 弱酸性次亜塩素酸水の噴霧による浮遊ウイルスの抑制性能評価試験
- バイオクリーンルームにおける微生物対策予ー次亜塩素酸水の検証を中心にー
- 次亜塩素酸水溶液の効能 ・ 空間噴霧の効果と安全性
- 世界初!次亜塩素酸水の空間噴霧の安全性がヒトを用いた臨床試験で確認される
また、実際のオフイスでの使用報告としては沖縄県環境科学センターによる「
次亜塩素酸水噴霧による除菌試験
」が大変興味深いものとなっています。この報告を参考にすれば:
■人が居ない時間帯に次亜塩素酸水を噴霧して部屋全体を除菌すれば人体への悪影響を回避できる
のでお勧めです。人のいる時に噴霧する場合は空気中塩素濃度が作業環境許容濃度(0.5ppm)を十分下回るよう注意することは当然として:
■そこにいる人全員が塩素臭や喉への違和感を感じない程度の噴霧量におさえる
■塩素過敏症の人が一人でもいる場合は噴霧しない
といった基準を設けて遵守すべきです。

次亜塩素酸水は良いことばかりであるように説明してきましたが、使用するにあたっては注意しなければいけないこともあります。
- 名前の似ている次亜塩素酸ナトリウムとは別物なので、決して取り違えないでください。
- 次亜塩素酸水と称して販売しているものであっても、製造法や組成はまちまちで、副次的(余計)な成分が入っているものもあります。 信頼のおける会社が電解法で製造し、有効塩素濃度などの規格を明確に表示してあるものを使用なさることをお勧めします。
- 次亜塩素酸はとても不安定な物質で、高い熱や強い光にさらされると数日持たずに分解して効果がなくなることもあります。 効果の失われたものを有効と信じて使用するのはとても危険ですので、次亜塩素酸水には消費期限があるものとして取り扱い、さしあたって使用しない場合は密閉容器に入れて、冷暗所で保存してください。 (保存方法については下記「次亜塩素酸水の保存期間」をご覧ください)
- 次亜塩素酸水の有効成分は次亜塩素酸(HClO)で、その効力は有効塩素濃度として測定できます。 有効塩素濃度が高いものほど除菌能力も高いのですが、高すぎると皮膚などに対する刺激が強くなります。
- 次亜塩素酸は、食物残渣などの有機物が多量にある場合はそれにより消費されてしまいますので、次亜塩素酸水で除菌する場合は有機物を洗浄した後に行うことになります。もちろん、洗剤を用いなければおちない油汚れなどを除けば、洗浄作業も次亜塩素酸水で行うことが可能です。
- 極めて大雑把になってしまうことを承知で言えば、有効塩素濃度が10~35mg/Lのものは布巾のつけ置き洗いや野菜の洗浄などにタップリ使い、35~60mg/Lのものは除菌力がある割に皮膚に与える刺激がほとんどないので手指の洗浄・除菌に、60~80mg/Lのものは水に濡れたものや微量の有機汚れが残っている場合にも効果があるので、包丁やまな板などの除菌に用いると良いと思います。
- 有効塩素濃度が80mg/Lを大きく超える次亜塩素酸水も市場に出回っています。このような高濃度の次亜塩素酸水は床や壁などの洗浄・除菌には使えますが、人体に対する安全性が確認されているものではありません。皮膚や粘膜などに対する刺激は有効塩素濃度に応じて強くなるので、素手では扱わない等、取り扱いには注意するべきです。

次亜塩素酸水の効力のところで、次亜塩素酸が酸化され易い有機物と接すると
HClO → HCl + O
のように分解して相手に酸素を与えると説明しましたが、実はそのような相手が身近にいなくても、この分解反応は常に起こっています。 分解したときに酸素を与える相手がいない場合には反応が逆に進んですぐに次亜塩素酸に戻ることもありますが、同時に発生した酸素原子同士が結合して酸素分子になることも一定の確率で起こります。この場合は:
2HClO → 2HCl + O2
という化学反応が起きたことになります。 この反応がゆっくり進むことにより、次亜塩素酸水は時間と共に有効塩素濃度を低下させ、効力を失っていきます。 これはしかたのないことですが、有効期間は次亜塩素酸水の保存環境により大きく変化しますので、どのような保存のしかたをすれば良いかをご説明します。
- どのような化学反応も温度が10℃上がれば反応速度が2倍になるといわれています。次亜塩素酸水の有効成分が低下するのは化学反応によるものですから、10℃で保存する場合は30℃で保存する場合に比べて有効期間が2倍の2倍、つまり4倍に延びるという計算になります。
- 次亜塩素酸の分解反応は強い光などの刺激によっても、促進されます。 夏場の直射日光にさらした場合、強い光と高温の両面攻撃によって、わずか一日で有効塩素濃度が0になったという★報告(山口県薬剤師会学校薬剤師部会研究委員会、2020)もあります。
- 温度などの環境条件が同じであれば、次亜塩素酸の濃度が高いほど分解反応が早く進むとされています。
- 次亜塩素酸分子には弱い揮発性があるため、ゆっくりと空気中に逃げ出します。そして空気中では不安定なため速やかに分解します。また、上に書いた 2HClO → 2HCl + O2 という化学反応式は次亜塩素酸が塩化水素と酸素に分解することを表していますが、この酸素も空気中に逃げ出します。密閉容器中であれば空気中の次亜塩素酸や酸素の濃度が上がりますので、これらの気体が水中から逃げ出しにくくなります。しかし、次亜塩素酸や酸素が気体として空気中へ容易に逃げ出すような状態であれば、水中の次亜塩素酸濃度はどんどん減少します(下図)。 つまり、容器の蓋を開けっ放しにすると次亜塩素酸水の寿命が縮むということです。
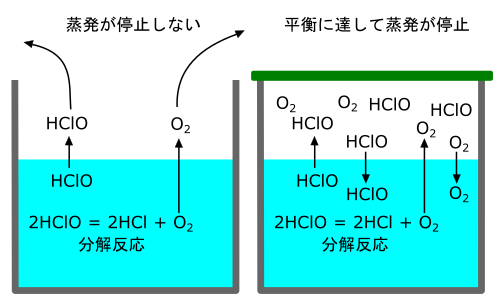
蓋の有無による次亜塩素酸濃度減少速度の違い
蓋がなければ(左図)次亜塩素酸と酸素が気体となってどんどん逃げだし、次亜塩素酸の水中濃度が下がり続けます。蓋がある場合は(右図)容器内空気中の次亜塩素酸と酸素が一定の濃度に達すると水から蒸発する速度と水に溶け込む速度が等しくなり、蒸発による水中濃度の減少が停止します。
蓋の重要性については、弊社が北見工業大学にやっていただいた次のような実験結果があります:
■有効塩素濃度30mg/Lのサンプルを無色透明のガラス瓶に入れ、蓋をせずに蛍光灯照射下で撹拌したところ、3時間後には大幅な濃度低下が見られ、15時間後には濃度ゼロとなった。
■同じ瓶で密栓をした状態で撹拌した場合、15時間後でも大きな濃度低下は見られなかった。
これほど極端な悪条件ではなく、容器(遮光瓶)の蓋を開けたままで実験室に放置した場合についても実例があります。 ★帯広畜産大学とアクトの連名で国際誌に掲載された研究報告に書かれていますが、有効塩素濃度100mg/L強のものが17日間放置で23mg/Lに、31日間放置で2mg/Lに低下したというものです。
ということで「使用したい有効塩素濃度(あるいはそれより少し高めの)次亜塩素酸水を、酸素ガスを通さない密閉容器に満杯に近い状態で入れ、光が当たらないようにして、低温で静かな所に置いておく」というのが最良の保管方法ということになります。 製造工程が良く管理されていて品質の良い(余計な成分が入っていない)次亜塩素酸水の場合、密閉容器に入れて10℃程度の温度で暗所保存した結果、2か月経っても有効塩素濃度が40mg/Lから30mg/L程度に落ちただけという弊社の実験結果があります。
以上のことから、保管条件さえよければ出荷時に有効塩素濃度が50mg/L程度の次亜塩素酸水は、2~3ケ月程度はアルコール消毒液の代わりに使えると言ってよいでしょう。
保存に関するもうひとつの注意点として、次亜塩素酸水をスプレーボトルに入れてしばらく放置した後の最初の一吹きは有効塩素濃度が容器の中のものより低いという弊社の実体験があります。種類にもよりますが、スプレーヘッドは密閉容器の蓋に比べるとガスを遮蔽する能力が落ちるため、スプレーヘッドの中に残っている次亜塩素酸の濃度が低下したものと考えられます。ですから、一定時間使わなかった場合は、1~2回目のスプレーで出てくる次亜塩素酸水は除菌効果が落ちていると考えた方が良いでしょう。
細心の注意を払っても「長期保存した次亜塩素酸水が何らかの理由で効力を失ってしまったのに、それで除菌をしたつもりで安心して、とんでもない結果になる」という可能性は否定できません。ですから、長期保存後の次亜塩素酸水を重要な用途に、例えば新型コロナウイルス対策として手など洗浄・除菌に用いたい場合※には、市販の測定器や試験紙などで有効塩素濃度を確認してからご使用いただくことを強くお勧めします。有効塩素濃度(塩分濃度ではありません)50mg/L(ppm)程度の測定に適したものをご選択ください。
※★(独)製品評価技術基盤機構の報告では有効塩素濃度35mg/L以上の次亜塩素酸水であればアルコール消毒液と同程度の効果があるとされています。
正確な測定をなさりたい場合は測定器の購入をすることになりますが、数万円の出費が必要となります。おおよその濃度を手軽に知りたいと思われる方には、試験紙の購入をお勧めします。例えば★この商品などはお手頃な価格で販売されています。

厚生労働省が指定する食品添加物としての次亜塩素酸水は食塩水などを電気分解して生成されたものと規定されています。上に述べた次亜塩素酸の不安定性のため、基本的には装置で製造後すぐに使用するものと想定されているからです。
ここでは食品添加物として使用可能な次亜塩素酸水を製造できる3種類の電気分解装置を紹介します。
電気分解装置には隔膜(イオン交換膜)の無いもの(一室型)、隔膜がひとつあるもの(二室型)、隔膜がふたつのもの(三室型)の3種類があります。
一室型電解装置による食塩水の電気分解
学校で行った水の電気分解実験では、電気を流れやすくするため、水に少量の水酸化ナトリウムを用いたことを覚えていますか。では、水酸化ナトリウム(NaOH)の代わりに塩化ナトリウム(NaCl、食塩)を溶かした水溶液を電気分解するとどうなるでしょう?
この場合、陰極では引き寄せられた過剰のナトリウムイオンにより水分子が水酸基(OH–)を奪われ、はじき出された水素イオン(H+)が陰極から電子を得るという反応が起きます。結果として陰極周辺では水素分子(H2)と水酸化ナトリウム(NaOH)が発生しますが、水素分子は水にほとんど溶けないので、気体として空気中に逃げていき、水酸化ナトリウムだけが溶液中に残ります。
2Na+ + 2H2O → 2NaOH + 2H+
2H+ + 2e– → H2 (eは電子)
一方、陽極では引き寄せられた塩素イオン(Cl–)が陽極に電子を奪われて塩素分子(Cl2)が発生しますが、この塩素分子は反応性が高いので、すぐに水分子と反応して塩化水素(HCl)と次亜塩素酸(HClO)ができます。(4OH– → 2H2O + O2 という、酸素分子ができる反応も少し起きます)。
2Cl– → Cl2 + 2e–
H2O + Cl2 → HCl + HClO
食塩水の電気分解によって次亜塩素酸ができるしくみがおわかりいただけましたでしょうか。
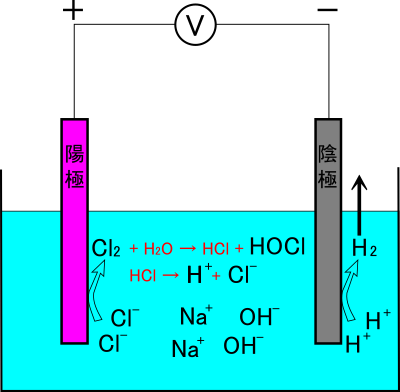
一室型の装置による食塩水の電気分解
以上のような、酸と塩基を作る反応が同時進行している反応全体を総合的に見ると、次のような反応式で表すことができます。
2NaCl + 3H2O → 2NaOH + HCl + HClO + H2
ここで発生する水素分子(H2)は速やかに空気中に逃げていきます。 そして、最終的に装置の電源が切られれば、二つの電極の間に仕切りがないため電解水全体が混ざり合い、陰極側で発生した水酸化ナトリウム(NaOH)1分子と陽極側で発生した塩化水素(HCl)1分子が反応して水と塩化ナトリウムになります。
NaOH + HCl → NaCl + H2O
結果として、溶液中に残るのは次亜塩素酸、水酸化ナトリウム、塩化ナトリウムの3成分ですので、生成した電解水はアルカリ性になります。つまり、一室型電解装置で食塩水を電気分解したときの物質全体の収支は次のようになります。
NaCl + 2H2O → NaOH + HClO + H2
ここで、下の図と説明を見てください。この図はpHが高くなればなるほど次亜塩素酸が水素イオン(H+)と次亜塩素酸イオン(ClO–)に解離する割合が増えることを示しています。上に書いたように次亜塩素酸(分子)の殺菌力は次亜塩素酸イオンの約80倍と言われていますので、アルカリ性の溶液中では除菌能力が大きく減少してしまいます。
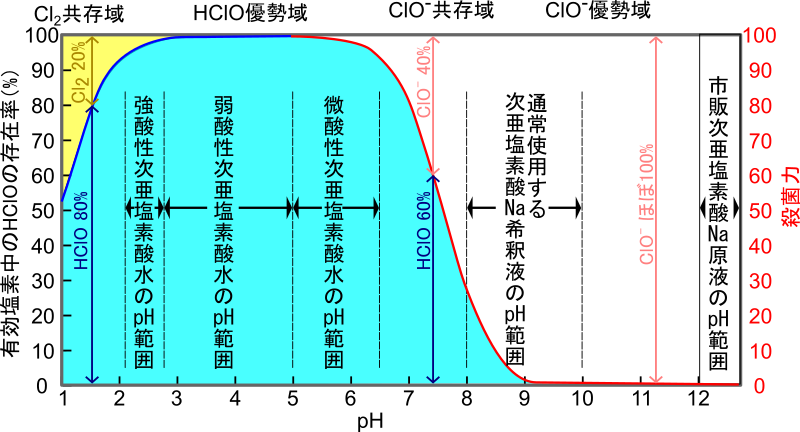
25℃における有効塩素中のHClOの存在比率のpH依存性。
ここで重要なことは、ClO–の殺菌力はHClOより二桁程度低いため、有効塩素濃度が同じであれば、pH5での殺菌力を100とした時、pHが高くなつにつれ、ほぼ赤線に沿って殺菌力(右側の目盛)が低下します。従って、有効塩素濃度が50ppmの次亜塩素酸水と同程度の殺菌力をもつ次亜塩素酸ナトリウム水溶液の有効塩素濃度は、pHが8の場合は150ppm以上、pHが9以上の場合は約5,000ppm(0.5%)にもなりますので、このような高濃度の有効塩素を含む水は取り扱いに注意が必要となります。
このような理由で、厚生労働省が定義する「一室型の電解装置による微酸性次亜塩素酸水」を得るためには、食塩(塩化ナトリウム)のかわりに(あるいは食塩に加えて)塩酸(塩化水素水溶液)を水に入れて電気分解し、pHを5~6.5の間に調整する必要があるのです。 原料として塩化水素を用いれば、全体の物質収支は:
HCl + H2O → HClO + H2 ↑
となりますから、生成する電解水は微酸性となります。 この方法により、反応前のHCl濃度と反応の進行程度を調節すれば、有効塩素濃度を10~80mg/L、pHを5~6.5の範囲に収めることができます。 これが「厚生労働省が食品添加物として規定する微酸性次亜塩素酸水」です。 このようにして製造した微酸性次亜塩素酸水の主成分は次亜塩素酸と消費されずに残った塩化水素となります。
■二室型電解装置による食塩水の電気分解
二室型電解装置は電極の間をイオンを透過させる隔膜で仕切っています(図は陽イオンも陰イオンも通すバイポーラーイオン交換膜の場合)。 この名前は水槽が陽極側と陰極側の二つに分かれていることによります。 この装置では、最初は水槽のどちら側にも塩化ナトリウム水溶液が入れられます。 電気分解が進行すると陽極の周辺では塩素イオンが消費されて塩化水素と次亜塩素酸が濃縮し、消費された塩素イオンに見合った分のナトリウムイオンが隔膜を通って陰極側へ、塩素イオンが陽極側へ移動します。陰極周辺では水素イオンが消費されて水酸化ナトリウムが濃縮し、発生した水素は大気中に放出されます。
陽極での反応: 2Cl- + H2O → HCl + HClO + 2e-
陰極での反応: 2Na+ + 2H2O + 2e- → 2NaOH + H2↑
(e- は電子)
結果として陽極側では酸性、陰極側ではアルカリ性の2種類の電解水が得られますが、この酸性電解水が次亜塩素酸水です。しかし、全ての食塩(NaCl)が消費されるまで反応を進められないため、いずれの電解水にも食塩が混在することになります。
陽極側では次亜塩素酸(HClO)とほぼ同量の塩化水素(HCl)が発生しますので、反応を進ませるほど次亜塩素酸濃度(有効塩素濃度)が上がり、それと同時に酸性度があがり(pHが下がり)ます。結果として、電気分解装置を停止させた時に酸性電解水のpHが2.7以下であれば強酸性次亜塩素酸水、そうでなければ弱酸性次亜塩素酸水ができたということになります。
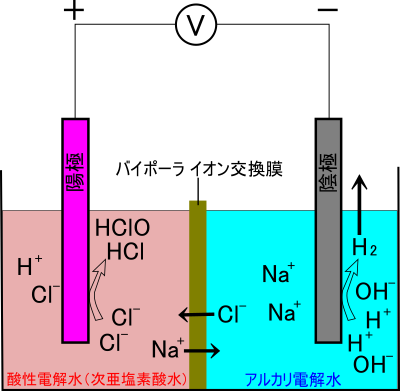
二室型の装置による食塩水の電気分解
三室型電解装置による食塩水の電気分解
三室型電解装置は電極の間を2枚の隔膜で仕切って、中央の室に食塩水を入れ、電極のある他の2室は純水のみをいれた状態から起働させるものです。この装置では陰極側の隔膜は陽イオンのみを、陽極側の隔膜は陰イオンのみを通すようになっています。つまり、ナトリウムイオンは陰極側にのみ、塩素イオンは陽極側にのみ移動可能です。この装置では電解を進めるに従って、それぞれの電極の周辺で二室型電解装置の場合と同じ反応が進行し、陽極側に酸性電解水が、陰極側にはアルカリ電解水が得られる点では二室型の電解装置と同様です。しかし、陽極側(酸性電解水)にはナトリウムイオンが存在せず、陰極側(アルカリ性電解水)には塩素イオンが存在しません。従って、食塩(NaCl)成分の無い「無塩型次亜塩素酸水」を得ることができます。
アクトの次亜塩素酸水製造装置「クリーン・ファイン」はこのタイプに相当します。
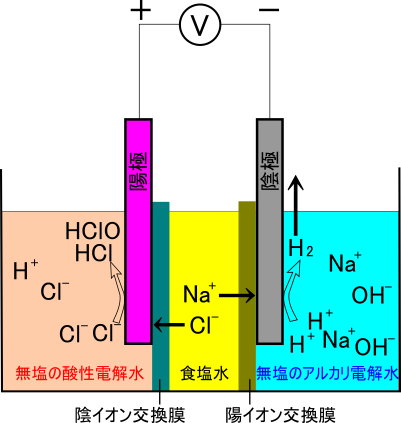
三室型の装置による食塩水の電気分解
クリーン・リフレについて詳しく知りたいお客様は>>>こちらです



